【东大新闻网4月4日电】(通讯员 张怡茹)3月29日,化学领域国际权威学术期刊《美国化学学会会志》Journal of the American Chemical Society在线发表了东南大学生物电子学国家重点实验室/生物科学与医学工程学院梁高林教授课题组的一项最新研究成果,论文标题为Apoptosis-Amplified Assembly of Porphyrin Nanofiber Enhances Photodynamic Therapy of Oral Tumor。该文章首次提出了一种“3A”策略(即:Apoptosis-Amplified Assembly,凋亡放大组装),设计了基于凋亡蛋白酶循环激活的多肽-卟啉分子Ac-DEVDD-TPP,实现了对口腔癌的自增强光动力治疗。(J. Am. Chem. Soc. 2023, DOI: 10.1021/jacs.2c13189)。
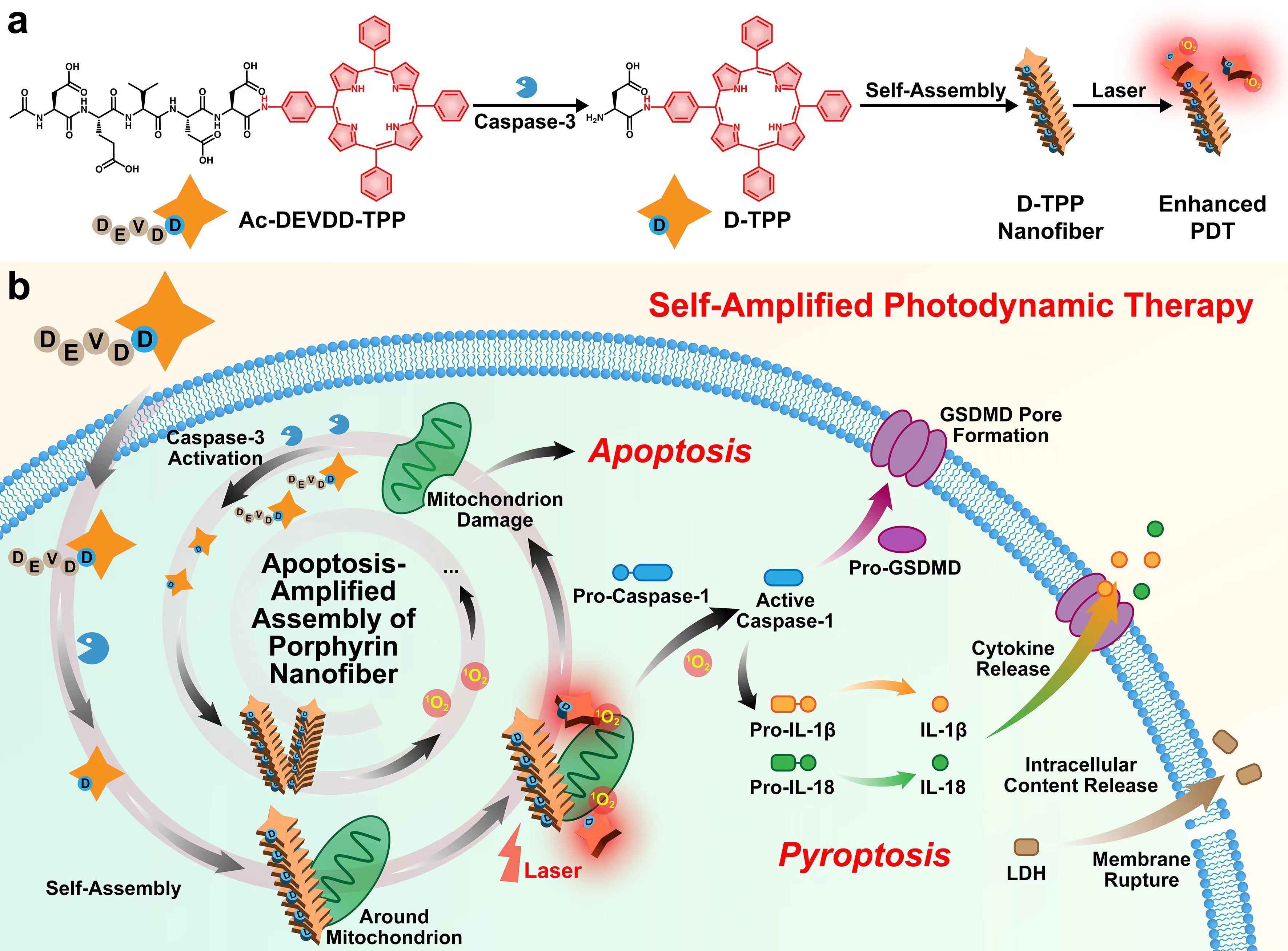
作为一种颇有前景的新兴技术,光动力治疗相较于传统的手术治疗及化疗方式具有高空间选择性的优势。但通常用于肿瘤光动力治疗的光敏剂分子往往水溶性较差且肿瘤选择性不足,从而极大制约了光动力治疗的疗效。针对这一科学问题,梁高林教授课题组设计出一种智能多肽-卟啉分子Ac-DEVDD-TPP(见图a)。该分子包含两部分,即凋亡蛋白酶半胱氨酸蛋白酶-3(Caspase-3)的多肽底物DEVD和具有自组装以及光动力能力的苯基卟啉结构。Ac-DEVDD-TPP分子进入肿瘤细胞后,经光/药物诱导产生的半胱氨酸蛋白酶-3识别并切割其底物序列DEVD生成D-TPP分子;D-TPP能够自组装形成D-TPP纳米纤维并聚集在线粒体周围;在激光照射下,D-TPP纳米纤维可产生更多的单线态氧、诱导细胞更深度凋亡、激活产生更多的半胱氨酸蛋白酶-3、从而实现凋亡放大组装的进程(见图b)。这种循环放大机制大大增强了癌细胞的凋亡过程,实现了肿瘤的增强光动力治疗。研究中发现,Ac-DEVDD-TPP分子在促进口腔癌细胞凋亡的同时还能够激活细胞焦亡通路,实现口腔癌细胞的协同高效杀灭。动物实验结果表明,该3A策略对口腔癌的皮下和原位模型具有显著增强的光动力治疗效果。
东南大学生物科学与医学工程学院博士生刘筱阳为该论文的第一作者。东南大学首席教授/生物电子学国家重点实验室副主任梁高林教授为唯一通讯作者。
该研究得到了国家自然科学基金重点项目和江苏省研究生科研与实践创新计划的资助。
附文章链接:https://doi.org/10.1021/jacs.2c13189
供稿:生物科学与医学工程学院

